亞太肝病醫學會APASL停止口服抗病毒用藥(NA)的指引【完整版】
亞太肝病醫學會是國際間最積極討論停藥的醫學會,提出停藥流程與注意事項。不想終身吃藥的朋友若已經知道停藥的風險,可以參考以下內容。若不清楚流程,建議先看最下方的停藥後選者。
陳建富醫師整理著作
1. 基本原則
APASL(亞太肝病研究學會)指引強調「個體化停藥」,必須符合以下 核心條件 才考慮停藥:
✅ HBeAg陽性患者:
- 已達成「HBeAg血清轉換」(HBeAg陰轉 + 抗-HBe陽性)
- 且 完成至少12個月的鞏固治療(HBV DNA持續<2000 IU/mL)
✅ HBeAg陰性患者:
- HBV DNA持續不可測(<2000 IU/mL)
- 且 完成至少3年的鞏固治療
⚠️ 絕對不建議停藥的族群:
- 失代償肝硬化(Child-Pugh B/C)
- 肝移植後免疫抑制患者
- HIV合併感染且未控制者
- 肝癌高風險(現有肝結節、家族史、血小板<100,000/μL)
2. 延伸考慮指標
APASL建議在基本條件外,進一步評估 附加預測因素,以提高停藥安全性:
(1) HBsAg定量(關鍵指標)
| HBsAg水平 | 停藥後HBsAg清除率 | 復發風險 |
|---|---|---|
| <100 IU/mL | 5年內可達30-50%[46] | 低(<20%) |
| 100-1000 IU/mL | 5年10-20% | 中(30-50%) |
| >1000 IU/mL | <5% | 高(>70%) |
實證依據:
- 台灣研究顯示,HBsAg <100 IU/mL 者停藥後的 3年持續緩解率達82%(vs. >1000 IU/mL僅28%)[100]
(2) HBV核心相關抗原(HBcrAg)
- <3 log U/mL:可作為額外安全性指標(日本研究顯示復發率降50%)[101]
- 適用於HBeAg陰性且HBsAg處於灰區(100-1000 IU/mL)的決策參考
(3) 肝纖維化程度
- 非肝硬化(F0-F3):可考慮停藥
- 代償性肝硬化(F4):
- APASL態度較保守,建議 無限治療
- 但部分研究支持 若符合所有條件(HBsAg<100 + 穩定超音波),可嘗試停藥[102]
3. 停藥後監測方案(APASL標準)
| 時間點 | 必檢項目 | 額外建議 | 異常處理 |
|---|---|---|---|
| 第1個月 | ALT + HBV DNA | HBsAg定量 | 若ALT>5×ULN + DNA陽性 → 考慮重啟 |
| 1-6個月 | 每月ALT + DNA | FibroScan(若肝硬化史) | DNA>2000 + ALT>2×ULN→ 討論治療 |
| 6個月後 | 每3個月ALT + DNA | AFP + 超音波(肝硬化者) | 新生結節 → 立即影像檢查 |
| 長期追蹤 | 每年HBsAg | 若HBsAg<10 IU/mL → 測抗-HBs | HBsAg清除者可降低監測頻率 |
⚠️ 重啟治療標準(APASL 2022更新):
強制重啟:
- HBV DNA >20,000 IU/mL + ALT >3×ULN
- 任何失代償證據(腹水、黃疸、凝血異常)
可選重啟:
- DNA >2000 + ALT >2×ULN 持續超過 12週
4. 特殊情境指引
(1) 使用低屏障藥物(LAM/ADV)者
- 若已長期病毒抑制(>5年),APASL建議 先換至高屏障藥物(ETV/TDF/TAF)至少1年 再評估停藥[103]
- LAM治療史者需 額外加測抗藥突變(rtM204V/I)
(2) 年輕患者(<40歲)
- 若符合條件,APASL認為可 更積極考慮停藥(因長期用藥毒性累積風險高)
- 但需確保 治療前非高病毒量(DNA <6 log) 並簽署知情同意[104]
(3) 合併代謝症候群者
- 糖尿病/脂肪肝患者停藥後 ALT發作風險增加2倍
- APASL建議此族群 HBsAg閾值應更嚴(<50 IU/mL)[105]
5. 證據等級與指引差異比較
| 項目 | APASL 2022 | EASL 2023 | AASLD 2023 |
|---|---|---|---|
| HBeAg(-)治療時長 | ≥3年鞏固 | ≥3年 | 不建議停藥 |
| 肝硬化停藥 | 不建議(F4) | 極特殊案例可考慮 | 絕對反對 |
| HBsAg閾值 | 強推<100 IU/mL | 未設標準 | 不列入條件 |
| 監測強度 | 首年密集 | 依風險調整 | 無具體規範 |
關鍵差異:
- APASL唯一明確將HBsAg定量納入停藥決策
- AASLD最保守,基本立場支持無限治療
6. 爭議與未來方向
(1) 爭議點
❌ HBsAg清除是否應為強制目標?
- APASL現行指引未強制要求,但 2025草案擬將「HBsAg<100 IU/mL」列HBeAg(-)停藥必要條件
❌ 鞏固治療3年是否足夠?
- 韓國研究顯示,HBeAg(-)患者治療>5年 者停藥復發率更低(30% vs 50%)[106]
(2) 新興指標研究
- 抗-HBc定量:>4.5 log IU/mL者停藥後控制較佳[107]
- HBV RNA:不可測(<100 copies/mL)可降低復發風險(OR=0.38)[108]
APASL停藥決策流程
1. 停藥初期監測階段(關鍵期)
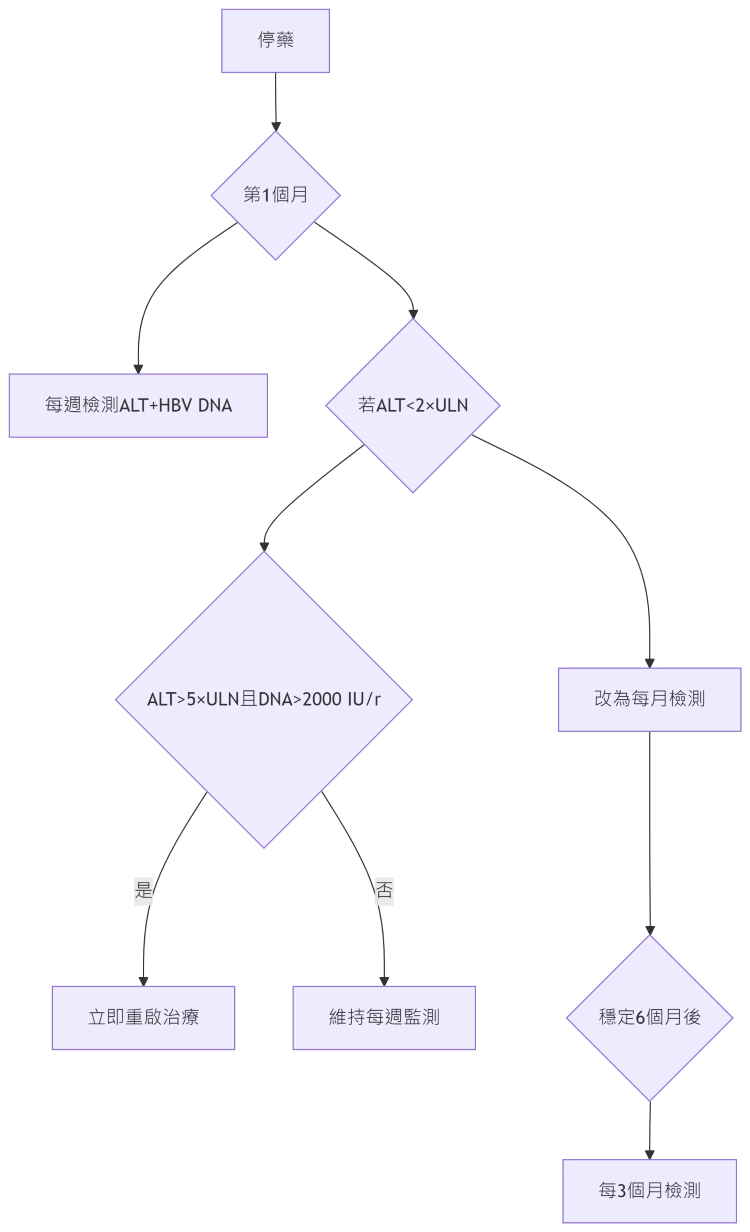
- 高風險患者監測流程:
- 停藥後第1個月:每週ALT + 每週HBV DNA
- 若ALT<2×ULN且DNA<2,000 IU/mL → 降為每月監測
- 任何ALT>5×ULN且DNA>2,000 → 立即啟動再治療
- 穩定6個月後 → 改為每3個月常規監測
- 肝硬化患者特別程序:
- 每月腹部超音波(前6個月)
- 每3個月檢測甲型胎兒蛋白(AFP)
- 任何新發肝結節立即進行對比增強影像檢查
2. 監測頻率調整標準
- 每週檢測:停藥後首月(高復發風險期)
- 每月檢測:需同時滿足:
- ALT持續<2倍正常值上限(ULN)
- HBV DNA<2000 IU/mL
- 每3個月檢測:連續6個月生化與病毒學皆穩定
3. 重啟治療指標
下列情況需立即恢復抗病毒治療:
- 病毒學反彈:HBV DNA>2000 IU/mL 且
- 生化反彈:符合任一條件:
- ALT>5×ULN
- ALT>2×ULN合併肝炎症狀(如黃疸、腹水)
- 肝硬化患者:只要偵測到病毒即應治療
4. 特殊族群注意事項
| 族群 | 監測要點 |
|---|---|
| 肝硬化 | ▸ 不建議自行停藥 ▸ 即使停藥,需終身每月監測 |
| HBeAg陽性 | ▸ 停藥後6個月內復發率達50% ▸ 建議加測HBeAg血清轉換 |
| 合併脂肪肝 | ▸ 需排除ALT升高是否由代謝因素引起 |
5. 長期追蹤建議
- 常規檢測:
- ▸ 每3個月:ALT、HBV DNA
- ▸ 每6個月:HBsAg定量、腹部超音波
- ▸ 每年:肝纖維化掃描(Fibroscan)
- 肝癌篩檢(高風險者):
- ▸ AFP(甲型胎兒蛋白)+ 超音波(每6個月)
重要臨床提醒
- 90%復發發生在停藥1年內,前3個月最需密集監測
- 假性正常化警訊:ALT輕微升高(2-5×ULN)可能先降後驟升,需搭配DNA變化判斷
- 所有檢測數值應以「同一實驗室基準值」比對
本流程參考2022年《APASL指南》與《台灣肝病醫學會建議》制定,實際臨床處置需依患者個別狀況調整。
APASL 2023 停藥標準專家解讀
✓ 理想候選人
- HBV DNA <20 IU/ml持續≥3年
- HBeAg陰性且anti-HBe陽性
- 超音波顯示無肝硬化跡象 (LSM <8 kPa)
- HBsAg <100 IU/ml且逐年下降
⚠ 需謹慎評估個案
- 合併代謝性肝病(MASLD)
- 有HCC家族史
- 停藥前HBsAg 100-1000 IU/ml
- 曾接受干擾素治療失敗者
核心臨床建議:
即使符合停藥標準,仍建議:
- 前6個月每月監測ALT/HBV DNA
- 每3個月定量HBsAg
- 繼續常規HCC監測
國際指南比較
| 標準 | APASL 2023 | EASL 2023 | AASLD 2022 |
|---|---|---|---|
| 停藥前最低治療年限 | 3年 | 無明確限制 | 1-2年 |
| HBsAg門檻 | <100 IU/ml (理想) | 無要求 | 無要求 |
「慢性B型肝炎停止抗病毒治療」完整系列:
- 慢性B型肝炎患者停止口服抗病毒用藥治療的指導方針
- 停止口服抗病毒用藥(NA)治療的優勢【完整版】
- 停止口服抗病毒用藥(NA)治療的風險【完整版】
- 停止口服抗病毒用藥(NA)的風險管理與臨床對策【專家版】
- 亞太肝病醫學會APASL停止口服抗病毒用藥(NA)的指引【完整版】(當前文章)
_100_100.webp) 預約掛號
預約掛號


 左右尚有資訊
左右尚有資訊